Периодический закон и периодическая система элементов Д.И. МенделееваСтраница
3
3
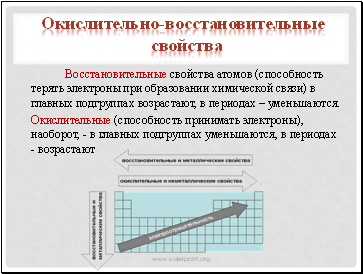
Поскольку окислительно – восстановительные свойства атомов оказывают влияние на свойства простых веществ и их соединений, то металлические свойства простых веществ элементов главных подгрупп возрастают, в периодах – убывают, а неметаллические – соответственно, наоборот – в главных подгруппах убывают, а в периодах – возрастают.
Слайд 14
Восстановительные свойства атомов (способность терять электроны при образовании химической связи) в главных подгруппах возрастают, в периодах – уменьшаются.
Окислительные (способность принимать электроны), наоборот, - в главных подгруппах уменьшаются, в периодах - возрастают
Слайд 15
Электроотрицательность
Электроотрицательность в периоде увеличивается с возрастанием заряда ядра химического элемента, то есть слева направо. В группе с увеличением числа электронных слоев электроотрицательность уменьшается, то есть сверху вниз. Значит самым электроотрицательным элементом является фтор (F), а наименее электроотрицательным – франций (Fr).
Слайд 16
Изменение радиуса атома в периоде
Радиус атома с увеличением зарядов ядер атомов в периоде уменьшается,т.к. притяжение ядром электронных оболочек усиливается. В начале периода расположены элементы с небольшим числом электронов на внешнем электронном слое и большим радиусом атома. Электроны, находящиеся дальше от ядра, легко от него отрываются, что характерно для элементов-металлов
Слайд 17
В одной и той же группе с увеличением номера периода атомные радиусы возрастают. Атомы металлов сравнительно легко отдают электроны и не могут их присоединять для достраивания своего внешнего электронного слоя.
Слайд 18
Источники инфорации
О.С. Габриелян, И.Г. Остроумов Химия. Выпускной экзамен М. Дрофа, 2008.
П.А. Оржековский Подготовка к ЕГЭ. Химия. Сборник заданий. М. Эксмо, 2011
Содержание
- Открытие Периодического закона
- Что же было обнаружено?
- Периодическая закон Д.И. Менделеева
- Первый вариант Периодической таблицы
- Периодическая таблица Д.И. Менделеева
- Периодическая таблица химических элементов
- Окислительно-восстановительные свойства
- Электроотрицательность
- Изменение радиуса атома в периоде
Последние добавления
- 10 способов улучшить свою жизнь
- Менеджмент в сестринском деле теория и практика
- Автотранспорт
- Археология
- Что такое деньги
- Австралия
- Интеграция различных подходов к менеджменту